Ein Blutgefäß ist im Prinzip ein Schlauch, durch den Blut fließt. Er wird von der Gefäßwand gebildet. Die Wand größerer Blutgefäße besteht aus drei aufeinander liegenden Gewebeschichten:
- innere Gefäßschicht (Intima),
- mittlere Gefäßschicht (Media) und
- äußere Gefäßschicht (Adventitia)
Der Hohlraum im Inneren eines Gefäßes wird als Lumen bezeichnet.
Zu einer Aufspaltung der Gefäßwandschichten kommt es, wenn die die innere Schicht einreißt, aber die äußere Schicht intakt bleibt. Dann dringt Blut aus dem Lumen durch den Riss in den Raum zwischen den beiden Schichten ein.
Aufgrund des erhöhten Drucks, der in der Aorta herrscht, gelangt immer mehr Blut in die Zwischenschicht. Dadurch weichen die Schichten über weite Strecken auseinander und können einen unnatürlichen Zwischenraum bilden. Dadurch kann das eigentliche Lumen vollständig verschlossen werden.
Die Intima hält in der Regel dem hohen Druck nicht stand und reißt an einer anderen Stelle wieder ein. Dadurch kann das Blut in die Aorta zurückfließen.
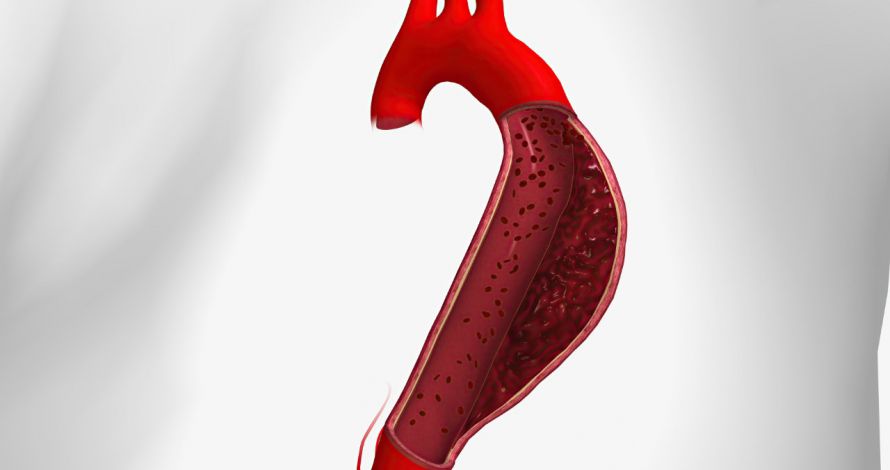
Darstellung einer Aortendissektion mit Blut im Zwischenraum der Aortengefäßwand © htcmed | AdobeStock
Als Risikofaktoren für die Entstehung einer Aortendissektion gelten Arteriosklerose und eine Strukturschwäche der Media (Mediadegeneration). Eine solche Strukturschwäche zeigt sich häufig bei Patienten mit angeborenen Herzklappenanomalien oder Bindegewebserkrankungen. Entsprechende Krankheiten sind etwa das Marfan-Syndrom oder das Ehlers-Danlos-Syndrom.
Weitere Risikofaktoren sind ein höheres Lebensalter sowie hoher Blutdruck. Daneben können traumatische Ereignisse ursächlich für eine Aortendissektion sein, etwa eine Verletzung der Gefäßwand bei einer Katheteruntersuchung.
Die Krankheitszeichen hängen von der Lage und dem Ausmaß der Dissektion ab. Manche Patienten mit chronischer Aortendissektion haben überhaupt keine Beschwerden. Bei anderen wiederum kann es im Extremfall bei einer Ruptur der Aorta zu einem plötzlichen Herztod kommen.
Typischerweise zeigt sich eine akute Aortendissektion durch einen plötzlich einsetzenden, heftigen, stechenden oder reißenden Schmerz in der Brust. Er kann bis in die Schulterblätter und den Rücken ausstrahlen.
Je nach betroffenem Gefäßabschnitt können weitere Symptome auftreten, wie beispielweise
Durch den Blutverlust kann es zu Symptomen des Schocks kommen, etwa
- beschleunigter Puls,
- Abfall des Blutdrucks,
- Bewusstseinstrübung.
Je nach Lage des Einrisses und Ausdehnung der Einblutung lassen sich mehrere Kategorien unterscheiden. Die DeBakey-Klassifikation definiert drei Typen von Aortendissektionen:
- DeBakey I: Einriss im Bereich der aufsteigenden Aorta (Aorta ascendens), die Einblutung reicht über den Aortenbogen hinaus.
- DeBakey II: Einriss ebenfalls in der Aorta ascendens, allerdings erfolgt der Wiedereintritt der Blutung noch in der Aorta ascendens.
- DeBakey III: Entry und Re-Entry liegen in der Aorta descendens (absteigende Aorta).
Eine Weiterentwicklung ist die Stanford-Einteilung. Sie unterscheidet anhand der Lokalisation des Entry lediglich zwei Typen:
- Stanford A (= DeBakey I und II): Einriss in der Aorta ascendens,
- Stanford B (= DeBakey III): Einriss in der Aorta descendens.
Die Lage des Einrisses ist entscheidend für die Gefährdung des Patienten und damit für die Therapie. Daher wenden die Spezialisten für Aortendissektion hauptsächlich die Stanford-Typen zur Beurteilung der Erkrankung an.
Bei Verdacht auf eine Aortendissektion können bildgebende Verfahren Einblutungen in die Aorta darstellen. Erste Hinweise können
geben. Die transösophageale Echokardiografie (TEE, Ultraschalluntersuchung über die Speiseröhre) ermöglicht eine genaue Beurteilung der herznahen Aorta sowie der Aorta descendens.
Die Dopplertechnik erlaubt zudem eine Unterscheidung des normalen und „falschen“ Lumens, Entry und Re-Entry können meist erkannt werden. Über eine Kontrastmittel-verstärkte Computertomografie (CT) lassen sich das Ausmaß und die Beziehung der Aortendissektion zu den benachbarten Gefäßen gut darstellen. Die Magnetresonanztomografie (MRT) ist ebenfalls eine zuverlässige Methode zur Diagnose der Aortendissektion. Auch die Angiographie (Methode zur Darstellung der Gefäße) kann wichtige Erkenntnisse liefern.
Entscheidend für die Therapie ist die Lage des Einrisses.
Eine akute Dissektion vom Typ Stanford A muss als Notfall betrachtet werden und sollte möglichst schnell operiert werden. Dabei wird der betroffene Gefäßabschnitt in der Regel entfernt und durch eine Gefäßprothese ersetzt.
Die Implantation von Gefäßprothesen in die Aorta bedeutet ein relativ hohes Risiko für den Patienten. Deswegen wird eine Dissektion vom Typ Stanford B zunächst abwartend therapiert. Das bedeutet, dass der Arzt die Entwicklung der Dissektion beobachtet. Erst bei Verschlechterung der Situation, zum Beispiel bei
- drohendem Verschluss von Gefäßabgängen,
- rasch zunehmendem Gefäßdurchmesser oder
- drohender Ruptur der Aorta,
leitet er eine Therapie ein.
Komplikationen wie verschlossene Gefäßabgänge behandeln Spezialisten für Aortendissektionwerden mithilfe von Kathetern. Mittels Stentimplantation kann die Gefäßwand stabilisiert und bei Bedarf ein künstliches Re-Entry angelegt werden. Das reduziert den Druck im „falschen Lumen“ und verringert damit die Gefahr einer Ruptur.
Die Behandlung des Schmerzes und die Senkung des Blutdrucks erfolgt medikamentös.















